Cùng xem Tính chất hóa học của Phi kim, ví dụ và bài tập – hóa lớp 9 trên youtube.
Phi kim có tính chất hóa học gì? ngoài tính chất vật lý là tồn tại ở 3 dạng rắn (S, P,…); lỏng (Br2); khí (Cl2,O2,N2,H2…); không dẫn điện, không dẫn nhiệt và nhiệt độ nóng chảy thấp,…
Vậy phi kim có những tính chất hoá học đặc trưng nào? chúng ta hãy cùng tìm hiểu chi tiết về tính chất hoá học của phi kim, vận dụng các tính chính chất hoá học này để giải một số bài tập điển hình về phi kim qua bài viết này.
Bạn đang xem: Tính chất hóa học của Phi kim, ví dụ và bài tập – hóa lớp 9
* Tính chất hóa học của phi kim:
- Tác dụng với kim loại
- Tác dụng với Hyđro
- Tác dụng với Oxi
Dưới đây là chi tiết về tính chất hóa học của Phi kim, chúng ta hãy cùng tìm hiểu.
I. Tính chất hóa học của Phi kim:
1. Tác dụng với kim loại
a) Nhiều phi kim tác dụng với kim loại tạo thành muối:
PTPƯ: Phi kim + Kim loại → Muối
Ví dụ: 2Na + Cl2 → 2NaCl
Fe + S → FeS
b) Oxi tác dụng với kim loại tạo thành oxit:
PTPƯ: Oxi + Kim loại → Oxit
Ví dụ: 2Cu + O2 → 2CuO
2Mg + O2 → 2MgO
2. Tác dụng với hyđro
a) Oxi tác dụng khí hyđro tạo thành hơi nước
PTPƯ: Oxi + H2 → H2O
Ví dụ: 2H2 + O2 → 2H2O
b) Clo tác dụng khí hyđro tạo thanh khí hiđro clorua
Ví dụ: H2 + Cl2 → 2HCl
H2 + Br2 → 2HBr
– Nhiều phi kim khác (C, S, Br2,…) phản ứng với khí hyđro tạo thành hợp chất khí.
3. Tác dụng với oxi
– Nhiều phi kim tác dụng với khí oxi tạo thành oxit axit
Ví dụ: S + O2 → SO2
4P + 5O2 → 2P2O5
4. Mức độ hoạt động hóa học của phi kim
– Mức độ hoạt động hóa học mạnh hay yếu của phi kim thường được xét căn cứ vào khả năng và mức độ phản ứng của phi kim đó với kim loại và hyđro.
– Flo, Oxi, Clo là những phi kim hoạt động mạnh (flo là phi kim hoạt động mạnh nhất). Lưu huỳnh, Photpho, Cacbon, Silic là những phi kim hoạt động yếu hơn.
|
>> có thể bạn muốn xem:
|
II. Bài tập về tính chất hóa học của Phi kim
Bài tập 5 trang 76 sgk hóa 9: Cho sơ đồ biểu diễn chuyển đổi sau:
Phi kim → oxit axit → oxit axit → axit → muối sunfat tan → muối sunfat không tan.
a) Tìm công thức các chất thích hợp để thay cho tên chất trong sơ đồ.
b) Viết các phương trình hóa học biểu diễn chuyển hóa trên.
* Lời giải bài tập 5 trang 76 sgk hóa 9:
a) Chất thích hợp là S, ta có sơ đồ sau:
S → SO2 → SO3 → H2SO4 → Na2SO4 → BaSO4.
b) Phương trình phản ứng:
S + O2 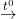
2SO2 + O2
2SO3
SO3 + H2O → H2SO4
H2SO4 + 2NaOH → Na2SO4 + 2H2O
Na2SO4 + BaCl2 → BaSO4↓ + 2NaCl
Bài tập 6 trang 76 sgk hóa 9: Nung hỗn hợp gồm 5,6g sắt và 1,6g lưu huỳnh trong môi trường không có không khí thu được hỗn hợp chất rắn A. Cho dung dịch HCl 1M phản ứng vừa đủ với A thu được hỗn hợp khí B.
a) Hãy viết các phương trình hóa học.
b) Tính thể tích dung dịch HCl 1M đã tham gia phản ứng.
* Lời giải bài tập 6 trang 76 sgk hóa 9:
– Theo bài ra ta có: nFe = 5,6/56 = 0,1 (mol); nS = 1,6/32 = 0,05 (mol);
a) Phương trình phản ứng:
Fe + S → FeS (1)
– Theo PTPƯ: nFe pư = nS = 0,05 mol ⇒ nFe dư = 0,1 – 0,05 = 0,05mol
nFeS = nS = 0,05 mol
– Nên hỗn hợp chất rắn A có Fe dư và FeS
Fe + 2HCl → FeCl2 + H2↑ (2)
FeS + 2HCl → FeCl2 + H2S↑ (3)
b) Dựa vào phương trình phản ứng (2) và (3), ta có:
⇒ nHCl = 2.nFe + 2.nFeS = 2. 0,05 + 2. 0,05 = 0,2 mol
⇒ VHCl = n/CM = 0,2/1 = 0,2 lít.
Bài 10 trang 81 sgk hóa 9: Tính thể tích dung dịch NaOH 1M để tác dụng hoàn toàn với 1,12 lít khí clo (đktc). Nồng độ mol của các chất sau phản ứng là bao nhiêu? Giả thiết thể tích dung dịch thay đổi không đáng kể.
* Lời giải bài 10 trang 81 sgk hóa 9:
Theo bài ra, ta có: nCl2 = 1,12/22,4 = 0,05 mol.
Phương trình phản ứng:
Cl2 + 2NaOH → NaCl + NaClO + H2O
Xem Thêm : Cách phân biệt các loại biển số xe từ 1/8/2020
Theo PTPƯ: nNaOH = 2.nCl2 = 2. 0,05 = 0,1 (mol)
VNaOH = n/CM = 0,1/1 = 0,1 lít
nNaCl = nNaClO = nCl2 = 0,05 mol.
CM (NaCl) = CM (NaClO) = 0,05 / 0,1 = 0,5 M.
Bài 11 trang 81 sgk hóa 9: Cho 10,8g kim loại M có hóa trị III tác dụng với clo dư thì thu được 53,4g muối. Hãy xác định kim loại M đã dùng.
* Lời giải bài 11 trang 81 sgk hóa 9:
Gọi M là khối lượng mol của kim loại (do kim loại hóa trị III nên khi phản ứng với Clo thì tạo thành muối MCl3), ta có PTPƯ sau:
2M + 3Cl2 → 2MCl3
10,8 g 53,4 g
Theo PTPƯ: nM = nMCl3 ⇒ 10,8/M = 53,4/(M + 35,5.3)
⇒ M = 27 (g). Vậy M là nhôm (Al)
Bài tập 5 trang 87 sgk hóa 9: Hãy xác định thành phần phần trăm về thể tích của mỗi khí trong hỗn hợp CO và CO2, biết các số liệu thực nghiệm sau:
– Dẫn 16 lít hỗn hợp CO và CO2 qua nước vôi trong dư thu được khí A.
– Để đốt cháy A cần 2 lít khí oxi. Các thể tích khí đo được ở cùng điều kiện nhiệt độ và áp suất.
* Lời giải bài tập 5 trang 87 sgk hóa 9:
– Dẫn hỗn hợp khí CO và CO2 qua nước vôi trong dư thu được khí A là khí CO, trong cùng điều kiện về nhiệt độ, áp suất thì tỉ lệ thể tích cũng bằng tỉ lệ về số mol.
– Phương trình phản ứng đốt cháy khí A:
2CO + O2 → 2CO2.
– Từ PTPƯ ta có: nCO = 2.nO2
⇒ VCO = 2.VO2 = 2.2 = 4 (l). (tỉ lệ mol cũng chính là tỉ lệ thể tích)
– Từ phương trình trên ta nhận thấy: VCO = 4 (l).
⇒ Vậy VCO2 = 16 – 4 = 12 (l).
⇒ % VCO2 = (12/16).100% = 75%;
⇒ %VCO = 100% – 75% = 25%.
Bài tập 5 trang 91 sgk hóa 9: Hãy tính thể tích khí CO2 (đktc) tạo thành để dập tắt đám cháy nếu trong bình chữa cháy có dung dịch chứa 980g H2SO4 tác dụng hết với dung dịch NaHCO3.
* Lời giải bài tập 5 trang 91 sgk hóa 9:
– Theo bài ra, ta có: nH2SO4 = 980/98 = 10 (mol).
– PTPƯ: 2NaHCO3 + H2SO4 → Na2SO4 + 2CO2 ↑ + 2H2O
– Theo PTPƯ: nCO2 = 2.nH2SO4 = 10.2 = 20 (mol).
⇒ VCO2 = n.22,4 = 20.22,4 = 448 lít.
Bài 5 trang 103 sgk hoá 9: a) Hãy xác định công thức của một loại oxit sắt, biết rằng khi cho 32g oxit sắt này tác dụng hoàn toàn với khí cacbon oxit thì thu được 22,4g chất rắn.
b) Chất khí sinh ra được hấp thụ hoàn toàn trong dung dịch nước vôi trong có dư. Tính khối lượng kết tủa thu được.
* Lời giải bài 5 trang 103 sgk hoá 9:
a) Gọi công thức của oxit sắt là: FexOy
– Phương trình hoá học của phản ứng:
FexOy + yCO → xFe + yCO2 (1)
Xem Thêm : 3 lý do tại sao không in tiền nhiều?
1 mol y mol x mol y mol
0,4/x 0,4 mol
– Theo bài ra thì: nFe = 22,4/56 = 0,4 (mol).
– Theo PTPƯ: nFexOy = 0,4/x (mol)
⇒ mFexOy = (56x + 16y). 0,4/x = 32 ⇒ x : y = 2 : 3
⇒ CT của oxit sắt có dạng (Fe2O3)n
⇒ Chỉ có n = 1 phù hợp, vậy ta có CTHH oxit sắt là: Fe2O3.
b) Khí sinh ra CO2
– PTPƯ (1) được viết lại như sau:
Fe2O3 + 3CO → 2Fe + 3CO2
CO2 + Ca(OH)2 → CaCO3↓ + H2O (2)
1 mol 1 mol 1 mol 1 mol
– Theo PTPƯ (1): nCO2 = (3/2).nFe = (0,4.3)/2 = 0,6 (mol).
– Theo PTPƯ (2) ⇒ nCaCO3 = nCO2 = 0,6 (mol).
⇒ mCaCO3 = 0,6.100 = 60 (g).
Bài 6 trang 103 sgk hoá 9: Cho 69,6g MnO2 tác dụng với dung dịch HCl đặc dư thu được một lượng khí X. Dẫn khí X vào 500ml dung dịch NaOH 4M thu được dung dịch A. Tính nồng độ mol của các chất trong dung dịch A. Giả thiết rằng thể tích dung dịch sau phản ứng thay đổi không đáng kể.
* Lời giải bài 6 trang 103 sgk hoá 9:
– Ta có: nMnO2 = 69,6/87 = 0,8 (mol).
VNaOH = 500ml = 0,5 lít ⇒ nNaOH = CM. V= 0,5.4 = 2 (mol).
– Phương trình phản ứng:
MnO2 + 4HCl → MnCl2 + Cl2↑ + 2H2O.
– Theo PTPƯ: nCl2 = nMnO2 = 0,8 mol.
Cl2 + 2NaOH → NaCl + NaClO + H2O.
– Ta có tỉ lệ: 0,8/1 < 2/2 ⇒ NaOH dư nên tính nNaCl và nNaClO theo nCl2
– Theo PTPƯ: nNaCl = nNaClO = nCl2 = 0,8 (mol).
⇒ CM(NaCl)= CM(NaClO) = 0,8/0,5 = 1,6 (mol/l).
– Theo PTPƯ: nNaOH pư = 2.nCl2 = 2. 0,8 = 1,6 (mol).
⇒ CM(NaOH) dư = (2-1,6)/0,5 = 0,8 (mol/l).
Hy vọng với phần hệ thống lại kiến thức về Tính chất hóa học của phi kim, ví dụ và bài tập ở trên hữu ích cho các em. Mọi thắc mắc cần được hỗ trợ, các em hãy để lại bình luận dưới bài viết. Chúc các em học tốt.
» Mục lục bài viết SGK Hóa 9 Lý thuyết và Bài tập
» Mục lục bài viết SGK Vật lý 9 Lý thuyết và Bài tập
Đăng bởi: DONGNAIART
Chuyên mục: Giáo Dục
Nguồn: https://dongnaiart.edu.vn
Danh mục: Tin tức
Lời kết: Trên đây là bài viết Tính chất hóa học của Phi kim, ví dụ và bài tập – hóa lớp 9. Hy vọng với bài viết này bạn có thể giúp ích cho bạn trong cuộc sống, hãy cùng đọc và theo dõi những bài viết hay của chúng tôi hàng ngày trên website: Dongnaiart.edu.vn